Sabões e Detergentes
De acordo com as solicitações dos meus alunos de laboratório, resolvi postar a respeito da nossa última aula sobre sabões e detergente.

Para saber mais consultem o link abaixo:
http://qnesc.sbq.org.br/online/qnesc12/v12a04.pdf

Se o sabão é feito de óleos e gorduras, como é capaz de limpar superfícies engorduradas? É uma pergunta curiosa, uma vez que a composição básica dos sabões é justamente as gorduras animais e os óleos vegetais, todos insolúveis em água, daí o porquê da água sozinha não limpar esses compostos.
Uma grande descoberta revolucionou a limpeza, através dela é possível limpar sujidades acumuladas. Tudo muito simples: a mistura de óleos (ésteres) com soluções alcalinas (hidróxido de sódio ou potássio) deu origem a um produto que se dissolve em água e retira gorduras. Estamos falando do sabão, acompanhe a equação que tornou possível sua produção:
Óleo + base → sabão + glicerol
Voltando à pergunta anterior, se óleos são insolúveis em água, como é possível retirá-los usando água e sabão? Graças ao caráter polar e apolar do sabão. Abaixo uma demonstração de como funciona a interação entre sabão, água e óleo.

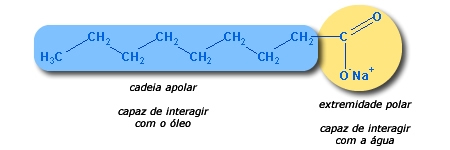
Repare que a molécula de sabão possui uma parte polar e outra apolar. A cadeia apolar formada por hidrocarbonetos (− CH2) se sente atraída por óleos (apolar) e a extremidade polar (contendo íons) interage com a água. Dizemos então que a molécula COONa é polar e hidrofílica (reage com água) e a cadeia de hidrocarbonetos é hidrofóbica (tem aversão à água). Essa força de atração é baseada na regra: “semelhante dissolve semelhante”.
Assim é possível que se forme uma emulsão (mistura) caracterizada pela espuma. É a partir dessa interação entre os componentes do sabão que se torna possível limpar superfícies cheias de gordura.
Para saber mais consultem o link abaixo:
http://qnesc.sbq.org.br/online/qnesc12/v12a04.pdf



Comentários
Postar um comentário